Dutasteride
más información sobre Avodart/Dutasteride/Avolve
de octubre 10 el 2002 el Avodart aprobado FDA, (Dutasteride)
el primer inhibidor del alfa-alpha-reductase 5 el dual-actuar
para la hiperplasia prostatic benigna (BPH)
Dutasteride fue aprobado por la autoridad reguladora sueca
(MPA) de julio el 24 de 2002. será puesto en Suecia por el
nombre comercial Avolve. El MPA acordó actuar como el Estado
miembro de la referencia para el procedimiento del
reconocimiento mutuo dentro de Europa y del plan de GSK para
poner la droga en todos los mercados europeos importantes
una vez que las aprobaciones se concluyan durante 2003. el
nombre comercial europeo (Avolve) debe ser confirmado.
Avodart (Dutasteride) se está lanzando para el tratamiento
de la próstata.
no está claro en el momento cuando Glaxo procederá con
ensayos de la pérdida del pelo.
Avodart debe estar disponible en diciembre de 2002.
efectos secundarios
- Dutasteride no se debe utilizar en mujeres y los niños.
las mujeres que son embarazadas o de pueden de llegar a ser
embarazadas no deben dirigir dutasteride debido a la
posibilidad de absorción el dutasteride y riesgo potencial
subsecuente a un feto masculino.
- los hombres trataron con dutasteride no deben donar
sangre hasta por lo menos seis meses después de su dosis
final para evitar el dar de dutasteride a una mujer
embarazada con una transfusión de sangre. los hombres con
una reacción alérgica al dutasteride o a sus ingredientes no
deben tomarlo. los hombres con enfermedad del higado deben
hablar con su doctor antes de tomar dutasteride.
- los ensayos clínicos del dutasteride demostraron que
estaba generalmente bien tolerado. la mayoría de los efectos
secundarios eran suaves o moderados e iban generalmente
ausentes mientras que en el tratamiento en los grupos del
dutasteride y del placebo.
- los efectos secundarios Droga-relacionados durante los
primeros seis meses eran como sigue: impotencia (4,7 por
ciento contra. 1,7 por ciento para el placebo), libido
disminuida (3 por ciento contra. 1,4 por ciento), dulzura
del pecho y ampliación del pecho (gynecomastia; 0,5 por
ciento contra. 0,2 por ciento) y desórdenes de la
eyaculación (1,4 por ciento contra. 0,5 porciento).
- la incidencia de los acontecimientos adversos sexuales
droga-ma's relacionados disminuyó con la duración del
tratamiento. la incidencia de la dulzura del pecho y de la
ampliación droga-relacionadas del pecho seguía siendo
constante sobre el período del tratamiento. el volumen de
Ejaculate se puede disminuir en algunos pacientes con el
tratamiento continuado. esta disminución no aparecía
interferir con la función sexual normal.
Dutasteride es el
primer inhibidor enzimático del reductase 5-alpha (ÄRI) que
inhibe ambos isoenzimas de los tipos 1 y 2. estas enzimas
son responsables de convertir la testosterona al
dihydrotestosterone en de (DHT) en la próstata, que se
demuestran desempeñar un papel dominante el desarrollo y
progresión BPH y pérdida del pelo.

las buenas
noticias son que los ensayos de la fase III se han
terminado ya para la hiperplasia benigna de Prostatic y
la droga ha sido dada la aprobación preliminar por el
FDA. se piensa que el dutasteride será vendido y el año
alguna vez próximo puesto. Finasteride siguió un curso
similar y primero fue aprobado para BPH y entonces más
adelante para la pérdida del pelo.

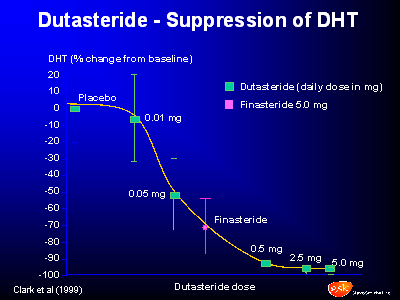
Dutasteride muy pequeño se requiere para inhibir el tipo
1 5-alpha-reductase pero las cantidades muy grandes de
Propecia se requieren para hacer tan. para el reductase
5-alpha del tipo 2 (los bloques de un Propecia), incluso
menos Dutasteride se requiere para bloquearlo que
Propecia. las dosis tan pequeñas de Dutasteride
proporcionan la inhibición muy buena de ambos tipos de
la enzima del reductase 5-alpha.
lo
más tarde posible lanzamiento de prensa
|
molécula del mes |
Lanzamiento De Prensa De Glaxo
|
Ensayos Clínicos |
Ensayos De Glaxo |
Más Info
|
