Dutasteride
Meer informatie over Avodart /
Dutasteride / Avolve
Op 10 oktober 2002 keurde de FDA Avodart goed, (Dutasteride)
de eerste tweevoudig-handelen 5 alfa-reductase inhibitor voor
goedaardige prostatic hyperplasia (BPH)
Dutasteride werd door de Zweedse regulerende autoriteit
(MPA) op 24 juli 2002 goedgekeurd. Het zal door de
handelsnaam Avolve op de markt in Zweden gebracht worden. De
MPA ging akkoord te handelen als de Referentie Lidstaat voor
de Wederzijdse Erkenning procedure binnen Europa en GSK plan
om op de markt het medicijn in alle belangrijke Europeaan
markten eenmaal goedkeuringen te brengen zijn tijdens 2003
afgerond. De Europese handelsnaam (Avolve) zal bevestigd
worden.
Avodart (Dutasteride) wordt voor de behandeling van de
prostaat vrijgegeven.
Het is niet helder nu wanneer Glaxo met haar verlies
pogingen zal doorgaan.
Avodart zou verkrijgbaar in december 2002 moeten zijn.
De zijde Bewerkstelligt
- Dutasteride zou in vrouwen en kinderen niet moeten
gebruikt worden. Vrouwen die zwanger zijn of zou zwanger
niet zou moeten behandelen dutasteride wegens mogelijkheid
van absorptie van dutasteride en verdere potentiële risico
naar een mannelijke foetus kunnen worden.
- Mannen behandelden met dutasteride niet zou moeten
schenken bloed tot tenminste zes maanden na hun laatste
dosis om te voorkomen gevend aan een zwangere vrouw
dutasteride door een bloed transfusie. Mannen met een
allergische reactie naar dutasteride of zijn bestanddelen
zouden het niet moeten nemen. Mannen met rechtstreekzere
ziekte zouden met hun dokter voor het nemen van dutasteride
moeten praten.
- Klinische pogingen van dutasteride toonden dat het
algemeen goed geduld werd. De meeste neveneffecten waren
zacht of matigt en wegging algemeen terwijl op behandeling
in zowel dutasteride als placebo groepeert.
- Drugsneveneffecten waren tijdens de eerste zes maanden
als volgt: onvermogen (4.7 procenten tegen. 1.7 procenten
voor placebo), afgenomen libido (3 procenten tegen. 1.4
procenten), borst gevoeligheid en borst uitbreiding
(gynecomastia; 0.5 procenten tegen. 0.2 procenten) en
ejaculatie stoornissen (1.4 procenten tegen. 0.5 procenten).
- Het voorkomen van de drugs seksuele ongunstige
gebeurtenissen nam met duur van behandeling af. Het
voorkomen van drugsborst gevoeligheid en borst uitbreiding
bleef constante over de behandeling periode. Ejaculeer
volume zal misschien afgenomen worden in sommige patiënten
met voortdurende behandeling. Deze afname is niet verschenen
zich met normale seksuele functie te bemoeien.
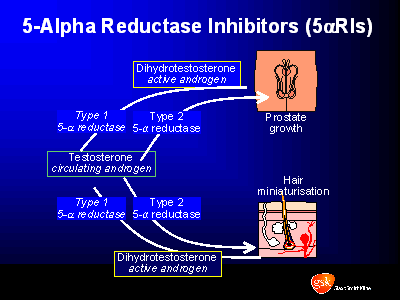
Dutasteride is het
eerst 5-alfareductase enzym inhibitor (5ARI) dat verbiedt
zowel typen 1 als 2 isoenzymes. Deze enzym zijn
verantwoordelijk voor het bekeren van testosteron naar
dihydrotestosterone (DHT) in de prostaat, die bewezen is om
een hoofdrol in de ontwikkeling en vooruitgang van BPH en
haar verlies te spelen.

Het goede
nieuws is dat Fase III pogingen reeds door de FDA voor
Goedaardige Prostatic Hyperplasia en het medicijn zijn
vervolledigd zijn aan voorafgaande goedkeuring gegeven.
Het is gedacht dat dutasteride op de markt ooit volgend
jaar zal verkocht worden en gebracht worden. Finasteride
volgde een gelijkaardige cursus en werd eerst voor BPH
en dan latere voor haar verlies goedgekeurd.
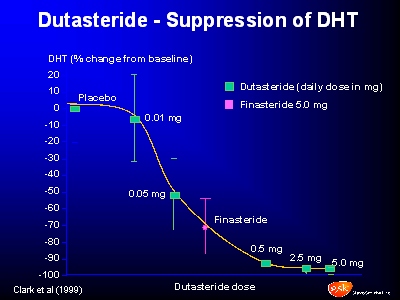
Heel
kleine Dutasteride is vereist type 1 5-alfa-reductase te
verbieden, maar heel grote hoeveelheden van Propecia
zijn vereist zo te doen. Voor type 2 zijn
5-alfareductase (de een Propecia blokken), zelfs kleiner
Dutasteride vereist het te belemmeren dan Propecia. Zo
kleine dosis van Dutasteride verzorgen heel goede
remming van beide typen van het 5-alfareductase enzym.
Laatste persvrijlating
| De
molecule van de Maande |
Glaxo Pers Vrijlating
|
Klinische Pogingen |
Glaxo
Pogingen |
Meer Info
|


.gif
)


